
特別企画
循環器デバイス治療の いま
第8回
潜因性脳梗塞における植込み型心電計による
早期心房細動検出と治療
—脳卒中医の立場から
岩手県立中央病院 脳神経内科 科長 土井尻 遼介 先生
潜因性脳梗塞とは
脳梗塞の病型は, 大きくアテローム血栓性脳梗塞, ラクナ梗塞, 心原性脳塞栓症, その他の脳梗塞, 原因不明の脳梗塞に分類される 1。このうち原因不明の脳梗塞のことを潜因性脳梗塞(cryptogenic stroke:CS)と呼び, その頻度は全体の16~39%と意外に多い 2。
CSの原因として注目されているのが, 入院中や外来時には指摘できない潜在性の発作性心房細動(paroxysmal atrial fibrillation:PAF)である。特に60歳以上のCS症例では, PAFが検出されやすい 3。潜在性のPAFの検出は12誘導心電図, ホルター心電図などの短期間のモニタリングでは困難であり, 測定時間を延ばすことにより検出される頻度が高くなる 4。そこで使用される機器が植込み型心電図モニタ(insertable cardiac monitoring:ICM)である。日本では, 2016年3月にCSに対するICMの使用が薬事承認された。日本脳卒中学会より植込み型心電図記録計の適応となり得る潜因性脳梗塞の手引きが作成されている 5。
潜因性脳梗塞の診断
CSは各種原因疾患を除外した病態である。したがって, 脳梗塞病型診断を正確に行わなければならない。Stop Stroke Study-Trial of Org 10172 in Acute Stroke Treatment(SSS-TOAST)分類 1によると, アテローム血栓性脳梗塞は脳梗塞に関連する頭蓋内外血管の50%以上の狭窄または閉塞病変が存在した場合, ラクナ梗塞は穿通枝領域に15~20mm以下の小梗塞を認めた場合, 心原性脳塞栓症は高リスク塞栓源心疾患(表1)を認めた場合に診断する。また, 奇異性脳塞栓症(深部静脈血栓症が卵円孔開存を通過する病態), 大動脈原性脳塞栓症(上行大動脈から大動脈弓部に4mm以上のプラークが塞栓源になる病態), 悪性腫瘍による脳梗塞(Trousseau症候群), 血管炎, 片頭痛, 血管れん縮, 薬剤不正使用, 血栓性素因による脳梗塞も存在する。以上の原因が除外された場合や検査不十分な症例, 原因が2つ以上存在する症例を原因不明の脳梗塞, 別名CSと診断する。なお, 2014年にHartらは潜因性脳塞栓症(embolic stroke of undetermined source:ESUS)の診断基準を提唱しており 2, アテローム血栓性脳梗塞, ラクナ梗塞, 心原性脳塞栓症, その他の脳梗塞を除外した疾患群である点はCSと類似しているが, 奇異性脳塞栓症や大動脈原性脳塞栓症などの原因は除外できておらず, CSよりも多くの疾患群を含む病態である。
CSと診断するには, 頭部MRIを使用してラクナ梗塞を否定すること, 頭頚部MRA, CTA, 脳血管撮影でアテローム血栓性脳梗塞を否定すること, 12誘導心電図, 24時間以上の心電図モニタでPAFによる心原性脳塞栓症を否定することが必須条件である。
日本脳卒中学会の手引き 5では経食道心エコーを推奨しているが, 同検査は左心耳内血栓の有無, 右左短絡検査, 大動脈プラークの有無を一度に観察できる非常に有用な検査である。しかし, 半侵襲的な検査であり, 嚥下障害のある患者や検査指示に従えない患者には施行が困難である。その場合は, 代替検査として造影CTで大動脈プラークを評価すること, 経胸壁心エコーもしくは経頭蓋超音波ドプラで右左短絡検査を行うことで, 奇異性脳塞栓症, 大動脈原性脳塞栓症をある程度は否定できる。また, 造影CTで全身の腫瘍の有無を確認することも重要である。右左短絡がある症例では, 下肢静脈エコーで深部静脈血栓症の有無を確認する。さらに, 脳血管炎や血栓性素因に関する血液検査も確認しておく。
CSは非心原性脳梗塞の再発予防に準じ, アスピリンをはじめとする抗血小板薬が第一選択となるが, CSは塞栓症であることが多く, 万が一PAFが検出された場合は直接阻害型経口抗凝固薬(direct oral anticoagulants:DOAC)へ再発予防薬を変更することができるため, CSではPAFの有無を突き止める必要がある。
表1 高リスク塞栓源心疾患

ICMの実際
ICMは原則ペースメーカ植え込み経験のある循環器内科医が行うことが多いと思われるが,植え込み手技は簡便であるため, 当院では循環器内科医の指導のもと, 脳神経内科医が自ら植え込みを行っている。挿入位置は各社どの機種も第4肋骨左縁付近に45度もしくは90度に植え込みを行うことが推奨されている。メスで10mm程度の切開を行い, 専用の付属された機器で挿入することができる。植え込み後1週間程度で創部は癒合し, 外見上, 特に目立つこともない。日常生活には支障なく, 1.5テスラのMRIにも対応可能である。
ICM挿入後は遠隔モニタから専用サーバーを介してPAFの有無を確認できるため, 患者が来院する必要はない。PAFが検出された場合, 設定したメールアドレスに通知が来るため非常に便利である。しかし, ICMにより自動検出されたPAFは偽陽性が問題となる。とくに持続時間が短いPAFは偽陽性が高いことが報告されており 6, 目視での診断が必要である。
ICMによるPAFの診断と治療方針
メドトロニック社のReveal™ XTを用いたICMモニタリングと標準的な心電図モニタリングでのPAF検出を比較したCRYSTAL AF試験では, ICM群で3年間のうち30%にPAFが検出された 7。参考までに,当院でのCSに対するICMのデータを紹介すると, 1年間に入院した急性期脳梗塞412例中, CSと診断してICMを施行した15例のうち, 1年以内に6例(40%)にPAFが検出された 8。また, 脳主幹動脈閉塞(major vessel occlusion:MVO)に対して血栓回収療法を施行した102例中, CS と診断してICMを施行した10例では1年以内に6例(60%)にPAFを認め 9, 日本脳卒中学会の手引きによって病型診断を行った急性期脳梗塞例, 脳主幹動脈閉塞のCS例では高率にPAFが検出されることが分かった。当院も参加した日本国内での多施設共同研究では, 約1年間でCS症例の26%にPAFがみられ 10, 海外からの既報告のPAF検出率よりも高率であった。MVOを伴うCS例では, 非MVO群と比較し, 3カ月以内のPAF検出率が有意に高率であった( 41% vs. 13%; P <0.01)。MVOはPAFの独立した予測因子となりうることが考えられ, ICMを積極的に使用し, PAFの検出に努めることが肝要と考える 11。
脳梗塞再発予防薬には抗血小板薬が処方されることが多く, 当院では, ICMでPAFを検出したらDOACへの変更を行っている。動悸を伴った有症候性のPAFであれば循環器内科へ紹介し, カテーテルアブレーションを施行している。
CS例に対しては, 脳卒中医がICM植え込みからモニタリングまで積極的に関わることによって, 真の病型を解明できると考えている。
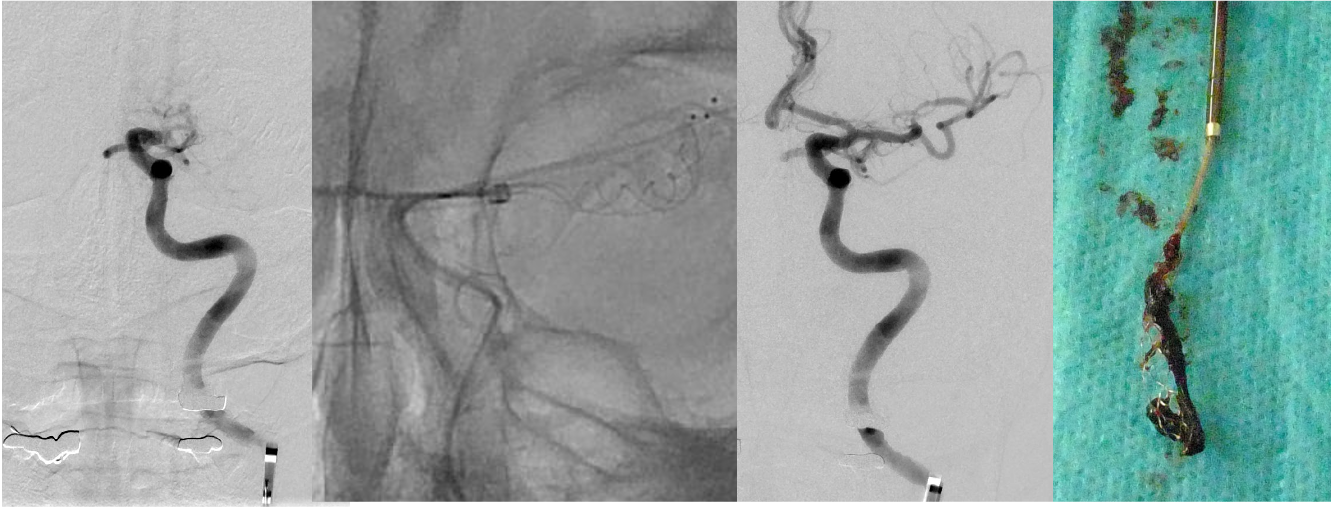
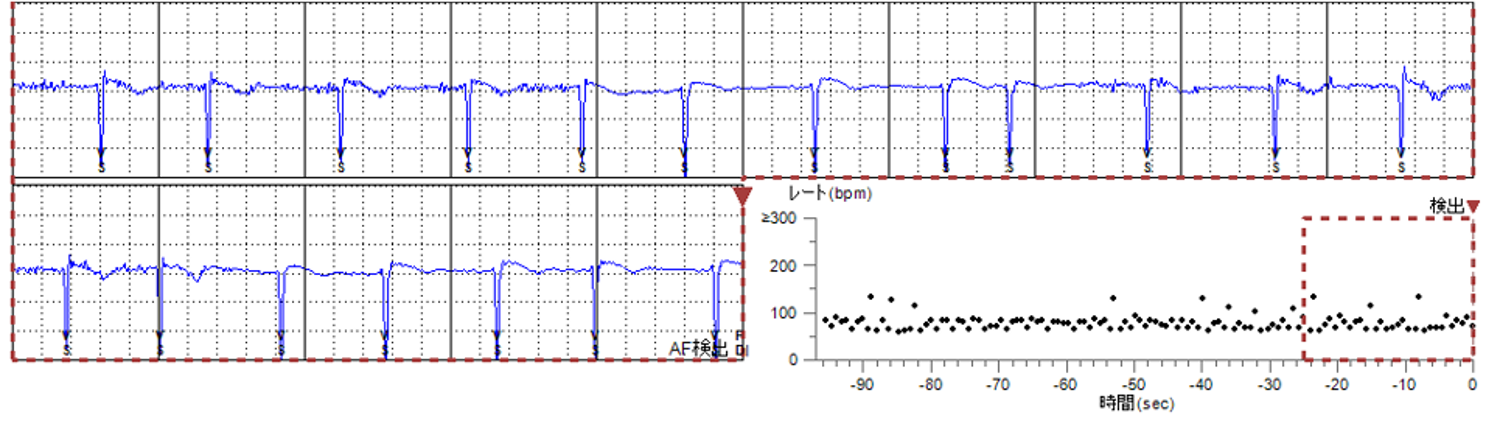
図1 脳主幹動脈閉塞例での潜因性脳梗塞の1例。65歳男性。来院時, 失語, 右片麻痺, NIHSSスコア21であった。12誘導心電図は洞調律であった。
参考文献
- Ay H, et al. An evidence-based causative classification system for acute ischemic stroke. Ann Neurol. 2005; 58: 688-697. PubMed
- Hart RG, et al. Embolic strokes of undetermined source: the case for a new clinical construct. Lancet Neurol. 2014; 13: 429-438. PubMed
- Verma N, et al. Incidence of atrial fibrillation among patients with an embolic stroke of undetermined source: Insights from insertable cardiac monitors. Int J Stroke. 2019; 14: 146-153. PubMed
- Sposato LA, et al. Diagnosis of atrial fibrillation after stroke and transient ischaemic attack: a systematic review and meta-analysis. Lancet Neurol. 2015; 14: 377-387. PubMed
- 日本脳卒中学会. 日本脳卒中学会 脳卒中医療向上・社会保険委員会 潜因性脳梗塞患者診断手引き作成部会. 植込み型心電図記録計の適応となり得る潜因性脳梗塞患者の診断の手引き. 2016年5月.
- Mittal S, et al. Real-world performance of an enhanced atrial fibrillation detection algorithm in an insertable cardiac monitor. Heart Rhythm. 2016; 13: 1624-1630. PubMed
- Sanna T, et al. Cryptogenic stroke and underlying atrial fibrillation. N Engl J Med. 2014; 370: 2478-2486. PubMed
- 土井尻遼介ら. 潜因性脳梗塞例に対する植込み型心電図記録計の導入と初期使用成績. 脳卒中. 2019; 41: 159-163.
- Doijiri R, et al. Treatment Outcome Using Insertable Cardiac Monitoring in Patients with Cryptogenic Stroke after Thrombectomy. Journal of Neuroendovascular Therapy. 2019; 13: 449-453.
- Iwata T, et al. High Detection Rate of Atrial Fibrillation With Insertale Cardiac Monitor Implantation in Patients With Cryptogenic Stroke Diagnosed by Magnetic Resonance Imaging. J Stroke Cerebrovasc Dis. 2019; 28: 2569-2573. PubMed
- Doijiri R, et al. Paroxysmal Atrial Fibrillation in Cryptogenic Stroke Patients With Major-Vessel Occlusion. Front Neurol. 2020 Nov 12; 11: 580572. PubMed
(c) copyright 2001-. Life Science Publishing Co., Ltd

